2022年9月16日-17日,第十二届中国胎儿医学大会成功举办。大会围绕胎儿疾病宫内诊断和治疗的新技术研发进展进行了汇报和成果分享。大会共设置了四大专题,邀请了众多来自生殖医学领域、胎儿医学领域的学术大咖在线进行交流研讨,受到广大专家学者的高度关注,学术交流成果斐然。
9月16日,第十二届中国胎儿医学大会在线上如期开幕,同日,会众生物卫星会也顺利召开,受到了来自产科、影像科、新生儿科、儿外科及医学遗传学等领域的专家学者的广泛关注。
本次卫星会以“脊髓性肌萎缩症在产前筛查与诊断的体会与思考”为主题,由来自深圳会众生物技术有限公司市场总监王笑迎主持,复旦大学代谢与分子医学教育部重点实验室副主任马端教授与上海市第一妇婴保健院胎儿医学科主任孙路明教授分别作了题为《脊髓性肌萎缩症(SMA)的发病机理》、《脊髓性肌萎缩症(SMA)的三级防控》的精彩分享。
脊髓性肌萎缩症简称SMA,虽然属于一种罕见病,但其在人群中的携带率高达1/40-1/50,发病率也达到1/6000-1/10000。若夫妻双方均为携带者,将有1/4的几率生育SMA患儿,给社会和家庭带来沉重的负担。
马端教授简要讲解了SMA的主要致病基因以及发病机制。SMA的主要致病基因是突变的SMN1,95%的SMN1突变形式是外显子7纯合缺失;SMN2与SMN1串联反相排列,属于假基因,与SMN1相比有5bp差异,其中1个存在于外显子7。
SMA致病基因SMN1编码的SMN蛋白是真核细胞生物生存所必需的管家蛋白。SMN作为亚单位与Sm蛋白结合,参与剪接体蛋白复合物的组装,调节mRNA的转运、代谢和翻译。同时,SMN还参与运动功能蛋白质的组装,与细胞的能量也有密不可分的关系。
如果SMN出现问题,除了影响多种基因的剪接,导致细胞出现死亡,出现退行性病变等情况以外,还会影响到很多细胞的功能,尤其是神经元功能,同时也会导致神经和肌肉连接部位出现问题。
马端教授还指出分析了SMN1与SMN2的不同之处:SMN1在没有突变的情况下,能够编码100%正确的蛋白,而SMN2在正常情况下,可以编码10%左右的正常蛋白。一旦SMN1出现突变,失去了编码蛋白质的功能,便依靠SMN2进行编码。因此SMN2拷贝数越多,编码的蛋白也越多。马端教授最后总结,临床上患儿的症状一方面与SMN1的突变有关,另一方面也与SMN2的拷贝数有关。
SMA作为一种严重致残,严重者致死的罕见病,遵循着出生缺陷三级防控的管理框架。孙路明教授指出,针对SMA的防控可分为三级预防。
一级防控,对于已经生育过SMA患者的高危家庭,应了解夫妻双方是否为携带者,做好SMA精准诊断。另外孙路明教授提到,由于SMA携带率较高,目前国内外指南的SMA共识,均建议表现健康人群在婚前检查或备孕时进行携带者筛查。
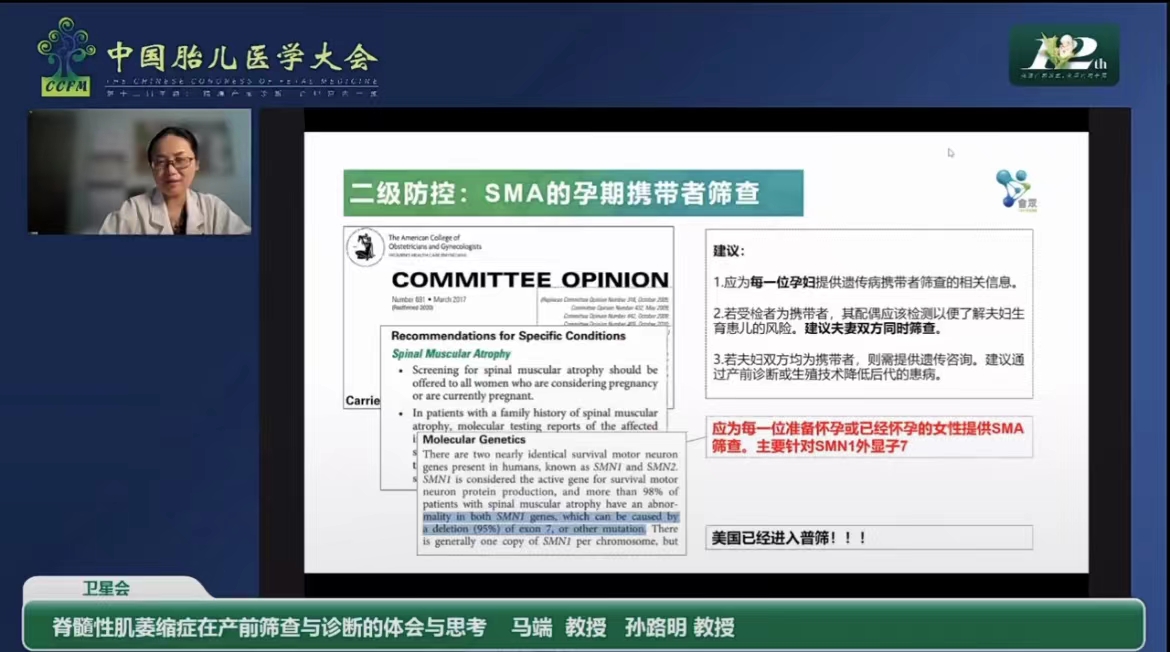
二级防控,应在早孕期为尚未进行SMA筛查的孕妇提供SMA筛查的相关信息,建议夫妻双方同时筛查。若夫妇双方均为携带者,则需提供遗传咨询,可通过产前诊断或生殖技术降低后代的患病。
孙路明教授提到,一般产检项目无法筛查出SMA。基于SMA发病的遗传机制,在孕早期进行SMA检测时主要针对SMN1的外显子7进行筛查。此外,孙路明教授认为,筛查并不是最终的诊断,应配备有完善的检测前的遗传咨询,需告知受检人可能出现的残余风险,尊重病人的知情选择权。
如果错过早孕期筛查,一般建议进行新生儿的筛查,即三级防控。新生儿的筛查指早期的筛查、干预,干预越早,SMA患儿预后效果越好。
孙路明教授最后总结,我们不可能避免所有SMA患儿的出生,但是三级防控能够减少SMA患儿的出生,减少SMA患儿的不良结局。
SMA所有临床前和临床研究表明,早期治疗干预,最好是症状前干预,可取得最佳效果。会众生物希望通过本次卫星会呼应国家对罕见病的关注,为我国出生缺陷防控、SMA诊疗事业贡献一份力量。